��֧��Flash
|
����Ԫ�صĵ��ʼ�����Ҫ������(��)
����4.���������Ľ���(�磺Fe��Al)
����(1)�˽������ͨ�Լ�����ұ����һ��ԭ���������˽�����Ļ��պ���Դ������
����(2)����Fe��Al�Ļ�ѧ���ʡ�
����(3)�˽ⳣ�������Ļ˳��
����(4)��Fe(��)��Fe(��)���ת��Ϊ���������۽���Ԫ�ص�������ԭ�ԡ�
����(5)�˽�������Ҫ�����
����(6)�����˽�Ͻ�ĸ��
����5.�˽�������������г�����������������ʺ���;��
����6.���ϸ�����֪ʶ���ۺ�Ӧ�á�
��������������������йع�ҵ������������ȷ����(����)
����A.�ϳɰ����������н�NH3Һ�����룬�ɼӿ�����Ӧ���ʣ����N2��H2��ת����
����B.���Ṥҵ�У��ڽӴ��Ұ�װ�Ƚ�������Ϊ������SO3ת��ΪH2SO4ʱ�ų�������
����C.��ⱥ��ʳ��ˮ���ռ�������ӽ���Ĥ�����ɷ�ֹ�����Ҳ�����Cl2����������
����D.��⾫��ͭʱ��ͬһʱ����������Һͭ����������������ͭ������С
�������𰸡�D
������������A�з���Һ��ֻ��ʹ�淴Ӧ�ٶȽ��ͣ�δӰ������Ӧ�ٶȡ�B���Ƚ���װ�����õ���SO2�������ų���������C��Cl2���������ɡ�D��⾫��ͭʱ�����������ʣ����ʽ���������ʧȥ���ӽ�����Һ��ͬʱͭ���ӵõ��������������������D��ȷ��
���������������ij����С���һЩ�������ʺͻ���������ʽ����о���
����(1)�±�Ϊ�������Ȼ�ͭ��Һ��Ӧ��ʵ�鱨���һ���֣�
|
ʵ�鲽�� |
ʵ������ |
|
����ĥ������Ƭ(����)����һ��Ũ�ȵ�CuCl2��Һ�� |
�������ݣ��������ɵĺ�ɫ���壬��Һ��Ϊ��ɫ |
|
��Ӧ������������Һ���� |
|
|
��ɫ����������ˮϴ�Ӻ����ڳ�ʪ������ |
һ��ʱ�������ɺ�ɫ��Ϊ��ɫ[������Ҫ�ɷ�ΪCu2(OH)2CO3] |
��������Ӧ����д��ʵ���з�����Ӧ�Ļ�ѧ����ʽ��һ��(�����ӷ�Ӧ��ֻд���ӷ���ʽ)
�����û���Ӧ��________________________________________________________________________��
�������Ϸ�Ӧ��________________________________________________________________________��
����(2)��ʯī���缫���������ʵ����������Һ�������������ݡ�������⣬��������������Һ�л����Թ۲쵽��������____________________�����ʹ���������ӷ���ʽ��____________________��
����(3)��ҵ�Ͽ����������̿�(��Ҫ�ɷ�ΪMnO2)��Ӧ��ұ�������̡�
���������������̿�ұ���̵�ԭ����(�û�ѧ����ʽ����ʾ)________________________________��
������MnO2��H2O2�ֽⷴӦ������������������MnO2�����ữ��H2O2����Һ�У�MnO2�ܽ����Mn2�����÷�Ӧ�����ӷ���ʽ��________________��
�������𰸡�(1)2Al��6H��===2Al3����3H2����2Al��3Cu2��===2Al3����3Cu
����2Cu��O2��H2O��CO2===Cu2(OH)2CO3
����(2)��ɫ�������ɣ���������ܽ�����ʧ
����Al3����3OH��===Al(OH)3��
����Al(OH)3��OH��===AlO2��2H2O
����(3)��3MnO2��4Al=�����£�3Mn��2Al2O3
������MnO2��H2O2��2H��===Mn2����O2����2H2O
�������������Ȼ�ͭ��Cu2������ˮ��ʹ��Һ�����ԣ�Cu2����2H2O���Cu(OH)2����2H�����������ᷴӦ����������2Al��6H��===2Al3����3H2��������Cu2�������û���Ӧ��2Al��3Cu2��===2Al3����3Cu�����ɵ��Ȼ�����Һ��⣬������������������ˮ�ĵ���ƽ�ⷢ���ƶ�������ʹ��Һ�Լ��ԣ�2Cl����2H2O===2OH����H2����Cl2�������ɵļ��������ӷ�Ӧ��Al3����3OH��===Al(OH)3����Al(OH)3��OH��===AlO2��2H2O������MnO2�����ữ��H2O2����Һ�У�MnO2�ܽ����Mn2�������ж�H2O2������ΪO2���÷�Ӧ�����ӷ���ʽ��MnO2��H2O2��2H��===Mn2����O2����2H2O��
���������������U��V��W��X��Y��Z��ԭ������������������ֳ���Ԫ�ء�Y�ĵ�����W2��ȼ�յIJ����ʹƷ����Һ��ɫ��Z��WԪ���γɵĻ�����Z3W4���д��ԡ�U�ĵ�����W2��ȼ�տ�����UW��UW2�������塣X�ĵ�����һ�ֽ������ý�����UW2�о���ȼ�����ɺڡ������ֹ��塣
������ش��������⣺
����(1)V�ĵ��ʷ��ӵĽṹʽΪ__________��XW�ĵ���ʽΪ__________��
����ZԪ�������ڱ��е�λ����__________��
����(2)UԪ���γɵ�ͬ��������ľ������Ϳ�����(�����)__________��
������ԭ�Ӿ��塡�����Ӿ��塡�۷��Ӿ��塡�ܽ�������
����(3)U��V��W�γɵ�10�����⻯���У�U��V���⻯��е�ϵ͵���(д��ѧʽ)__________��V��W���⻯����ӽ��H��������ǿ����(д��ѧʽ)__________����һ�����ӷ���ʽ����֤��____________________________��
����(4)YW2����ͨ��BaCl2��HNO3�Ļ����Һ�����ɰ�ɫ��������ɫ����VW���йط�Ӧ�����ӷ���ʽΪ____________________________________���ɴ˿�֪VW��YW2��ԭ�Խ�ǿ����(д��ѧʽ)__________��
�������𰸡�(1)NN��Mg2��[ ]2�����������ڵڢ���
����(2)�٢�
����(3)CH4��NH3��NH3��H3O��===NH4��H2O
����(4)3SO2��2NO3��3Ba2����2H2O===3BaSO4����2NO��4H����SO2
�����л���ѧ����
����1.�˽��л���������Ŀ�ڶ���칹�����ձ���ڵı���ԭ��
����2.������š������š�ͬ���칹�塢ͬϵ��ȸ���ܹ�ʶ��ṹʽ(�ṹ��ʽ)�и�ԭ�ӵ����Ӵ���ͷ�ʽ�����ź����š��ܹ�����ͬϵ����о�ͬ���칹�塣�˽�����������ԭ��
����3.��һЩ���͵��������Ϊ�����˽��л�������Ļ���̼�ܽṹ�����ո�����(������ϩ����Ȳ��������Ȳ)�и���̼̼����̼��������ʺ���Ҫ��ѧ��Ӧ��
����4.��һЩ���͵�����������(�Ҵ��������顢���ӡ���ȩ����ȩ�����ᡢ����������֬���ᡢ�����������ǻ�ȩ���������)Ϊ�����˽�������ڻ������е����á����ո���Ҫ�����ŵ����ʺ���Ҫ��ѧ��Ӧ��
����5.�˽�ʯ�ͻ�����ũ����Ʒ��������Դ�ۺ����ü���Ⱦ�ͻ����ĸ��
����6.�˽�������������г����л�������ʺ���;��
����7.��������Ϊ�����˽�����Ļ�����ɺͽṹ����Ҫ���ʺ���;��
����8.�˽⵰���ʵĻ�����ɺͽṹ����Ҫ���ʺ���;��
����9.�����˽���Ҫ�ϳɲ��ϵ���ҪƷ�ֵ���Ҫ���ʺ���;�������ɵ���ͨ���ۺϷ�Ӧ���ɸ߷��ӻ�����ļ�ԭ����
����10.ͨ�������������Ļ�ѧ��Ӧ�������л���Ӧ����Ҫ���͡�
����11.�ۺ�Ӧ�ø������IJ�ͬ���ʣ��������𡢼��������롢�ᴿ���Ƶ�δ֪��Ľṹ��ʽ����϶��������Ļ�ѧ��Ӧ���ϳɾ���ָ���ṹ��ʽ�IJ��
���������������������ݽ���������ѡ������л��ƶ�Ϊ�����ص��У��л����ȼ�չ��ɣ��л���Ӧ���ͣ������ŵ����ʺ�ת����ͬ���칹�����д�ȡ���ϰʱҪ��ϵ����������Ƽ�������������
�����������������ϸ�������б������������й��ɣ��ж������ڵ�15λ�����ķ���ʽ��(����)
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
���� |
|
C2H2 |
C2H4 |
C2H6 |
C3H4 |
C3H6 |
C3H8 |
C4H6 |
C4H8 |
C4H10 |
���� |
����A.C6H12 B.C6H14 C.C7H12 D.C7H14
�������𰸡�B
�������������۲죬������ÿ3��һ�飬�ظ���CnH2n��2��CnH2n��CnH2n��2(����n��m��1����һ��m��1)�ķ���ʽ����15λΪ��5���еĵ�3��������CnH2n��2�ķ���ʽ����n��m��1��5��1��6���ʷ���ʽΪC6H14��
���������������ç������һ�ֺϳ�����������ҩ���Ƶ�ԭ�ϣ����������ƻ������ʯ���ֲ���С����й����������л��������˵����ȷ����(����)
OHHOHOCOOH��OHHOHOCOOH
����A.�����ᶼ������ˮ��Ӧ
����B.�����������Ȼ�����Һ����ɫ
����C.���������ç���������ȶ�������̼̼˫��
����D.�����ʵ����������������������Ʒ�Ӧ��������������ͬ
�������𰸡�AD
������������ç�����к���̼̼˫����������ˮ�����ӳɷ�Ӧ�������з��ǻ���λ̼������ԭ�ӣ�������ˮ����ȡ����Ӧ��ѡ��A��ȷ��ç������������ǻ��������Ȼ�����Һ����ɫ��ѡ��B����������ӱ����е�̼̼��������̼̼ͨ˫�������ǽ��ڵ�����˫��֮���һ������Ļ�ѧ����ѡ��C����1 molç���ᡢ����ֱ���4 mol�ǻ��������������Ʒ�Ӧ���ɲ�������2 mol��ѡ��D��ȷ��
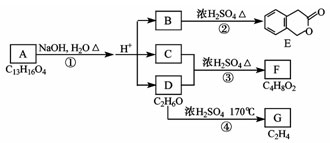
�����������������ͼ��A��B��C��D��E��F��G��Ϊ�л������
����������ͼ�ش����⣺
����(1)D�Ļ�ѧ������__________��
����(2)��Ӧ�۵Ļ�ѧ����ʽ��____________________��(�л������ýṹ��ʽ��ʾ)
����(3)B�ķ���ʽ__________��A�Ľṹ��ʽ��__________����Ӧ�ٵķ�Ӧ������__________��
����(4)��������3��������B��ͬ���칹����Ŀ��__________����
������)�����ڶ�ȡ�������ṹ����)��B����ͬ�����š���)����FeCl3��Һ������ɫ��Ӧ
����д����������һ��ͬ���칹��Ľṹ��ʽ��________________________________________________________________________��
����(5)G����Ҫ�Ĺ�ҵԭ�ϣ��û�ѧ����ʽ��ʾG��һ����Ҫ�Ĺ�ҵ��;��____________________��
�������𰸡�(1)�Ҵ�
����(2)CH3CH2OH��CH3COOH�D��Ũ�����CH3COOCH2CH3��H2O
����(3)C9H10O3
����CH2COOCH2CH3CH2OOCCH3��ˮ�ⷴӦ
����(4)3��COOHCHCH3OHCH3CHCOOHOHCOOHCH2CH2OH(��дһ������)
����(5)nCH2===CH2�D���������ȡ���ѹ��CH2��CH2��
������CH2===CH2��H2O�D���������ȡ���ѹCH3CH2OH(��дһ������)
������.����Ҫ��
����Ҫ����������Ϊ����������ѧ������ѧ��ؿγ̻���֪ʶ���������ܵ����ճ̶Ⱥ��ۺ�������ѧ֪ʶ��������������������Ҫ����������ϵʵ�ʣ���ע��ѧ��������ᾭ�ú���̬������Э����չ��Ҫ���ӶԿ�����ѧ�����Ŀ��顣
��������߿���Ϣ����ʣ����˸߿�Ƶ�� �߿���̳ �߿�����Ȧ �߿�����
�����ر�˵�������ڸ���������IJ��ϵ�����仯�����������ṩ�����п�����Ϣ�����ο������뿼����Ȩ�����Ź�������ʽ��ϢΪ��
�������
- �����š�һ��ɳ���С�
- ����ҹ�䵽���죬�㡭
- ����Ȼ���ʻ���λ��
- ��ʵ����Ƕ��Ӵ��ˡ�
- �����塿���簮��������
- I Need you
- ��ȹ �þò���
- ���� �Һ���
- ����������������
- ���㲻���
- ����� �ټ�
- �� ��������
- ��ͼƬ��ƽ�����
- ��������
- �������¼
- ѩ������ �����
��ҵ����
- ������֥--���ᣲ��������
- �����أ��������ֱ�������
- ��ȥ�۴�����Ȧ--������Ů
- ��˯������--�ݵ�����
- �����--����--��������
- ������--����--��ô�죿
- ���ڳ�--����--��ô�죿
- ����--�ѷ�--���²�����
- ��һ��һ������(ͼ)
- ���ڳ�--�ڳ�--��ô��?
- ��Ů�˸�����--��ô�죿
- ���������ϰ�Ϊ���
- ���������벻��������
- ����-�ѷ�---��ô�죿
- ��С��Ͷ�� ��òƸ�
- ������һ�����ڼ���Ǯ
| ���ĸ�30��30���б���Ǩ | �����ˡ��Ի����С� | �����к������ | �����������߸��Ż� |